- A+

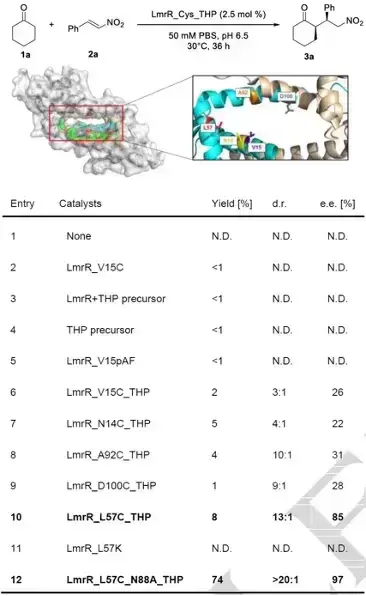
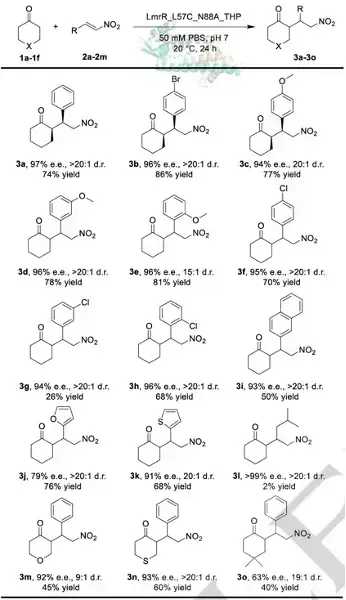
近年来,酶促不对称碳-碳键合成反应因其反应的温和性,高效性和高立体选择性而广受关注。但与合成化学中丰富多样的碳-碳键构建方法相比,生物酶法比较受限。为了开发高效的生物催化剂以应对具有挑战性的生物转化,需要不断引入新功能酶元件。借鉴有机化学中的催化模式可能有助于设计具有新功能的酶元件。 基于化学合成中成熟的胺催化策略,研究人员开发和改造了多种生物酶用于醛类化合物的不对称合成,但是相比之下,生物催化中实现酮分子的不对称合成报道较少,可能是由于酮比醛的反应活性更低。因此设计新酶实现酮类分子的不对称合成具有重要的研究意义。 近日,江南大学周志教授课题组设计并开发了一种以仲胺为催化中心的新型人工酶,该酶新设计的四氢吡咯催化中心以烯胺催化模式高效实现了环状酮分子与硝基烯烃的不对称迈克尔加成反应,并通过酶定向进化获得了优异的催化活性和立体选择性(97% e.e., >20:1 d.r., 86% yield)。 作者基于LmrR蛋白,通过二硫键共价修饰引入含有四氢吡咯的催化残基,以此构建仲胺为催化中心的人工酶酶库。通过酶定向进化,筛选出LmrR_L57C_N88A_THP突变体,可实现对模板反应97% e.e., >20:1 d.r.和74%产率。酶促动力学研究显示进化变体kcat/KM约为野生型L57C_THP的3.7倍,TTN约为野生型4倍。底物谱考察中,该进化变体对六元环状酮与各类取代芳基、杂环的硝基烯烃均显示出良好的耐受性,底物谱可拓展性强。半制备级别实验中,该人工酶同样可以实现略低于测试反应的手性控制与产率。 这项工作为手性酮化合物的合成提供了一种有效的生物催化策略,此种新设计的含有吡咯烷的人工酶可广泛适用于酮类分子的非天然生物催化反应开发,证明了人工酶设计在实现非天然反应中的巨大潜力。 论文信息 Design and Evolution of an Enzyme for the Asymmetric Michael Addition of Cyclic Ketones to Nitroolefins by Enamine Catalysis Zhixi Zhu, Qinru Hu, Yi Fu, Yingjia Tong, Zhi Zhou 该研究第一作者为江南大学生命科学与健康工程学院博士研究生朱致熹,通讯作者为江南大学生命科学与健康工程学院周志教授。 Angewandte Chemie International Edition DOI: 10.1002/anie.202404312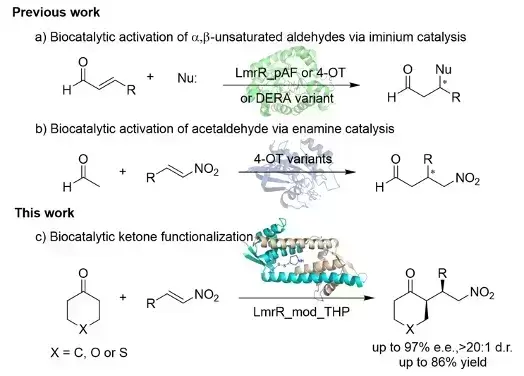


目前评论: