- A+
分享的是一篇近期发表在期刊 JACS 上的文章。文章标题是“Sialylation Shields Glycoproteins from Oxidative Stress: Mechanistic Insights into Sialic Acid Oxidation and Structural Stability”,本文的通讯作者是来自南开大学化学学院的李功玉特聘研究员(研究方向:D-蛋白质谱分析)和付浩浩副研究(研究方向:分子模拟增强采样算法和自由能计算)。
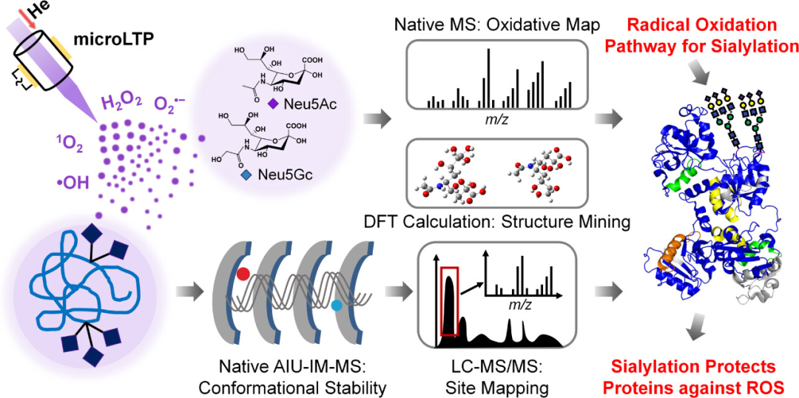
唾液酸化是一种常见的蛋白质翻译后修饰,发生在糖蛋白的 N- 和 O-糖末端。已发现的唾液酸在细胞分化、细胞增值、细胞凋亡、细胞间通信和免疫反应等多种生命活动中发挥重要作用。正常情况下蛋白质处于动态平衡状态,但氧化应激会导致蛋白质的结构破坏和功能失调,从而引发包括癌症、神经退行性疾以及代谢紊乱在内的多种疾病。蛋白质应对氧化应激的机制尚不完全清楚,唾液酸化被认为可以在一定程度上可以缓解氧化应激带来的损伤,但其具体机一直未被完全阐明。 在本文中,作者通过一种微尺度低温等离子体(microLTP)装置,模拟了细胞中复杂的氧化应激环境,并结合高分辨率质谱分析(MS)和密度泛函理论(DFT)计算,首次完整绘制了两种常见唾液酸(Neu5Ac 和 Neu5Gc)在自由基氧化条件下的氧化路径图。并进一步使用人转铁蛋白(hTF)作为模型,根据一系列 LC-MS/MS 位点定位、唾液酸化特异性酶处理和 AIU-IM-MS 技术,确定了特定蛋白质的结构基序和唾液酸化模式。(Scheme 1) Scheme 1. 深度自由基氧化揭示了末端唾液酸化对蛋白质氧化保护作用的分子基础 microLTP 衍生的 ROS 的表征 作者设计了一个 microLTP 装置,使用氦气作为载体气体生成了多种 ROS,包括羟基自由基(•OH)、超氧阴离子(O₂⁻)、单线态氧(¹O₂)和过氧化氢(H₂O₂)。随后,使用 EPR 波谱和其他分析技术对其产生的 ROS 进行了系统表征,结果显示 H₂O₂ 和 ¹O₂ 是主要的 ROS,浓度范围分别为 10–180 μM 和 24–240 μM,而 O₂⁻ 和 •OH 的浓度较低,分别为 40–120 μM 和 1–28 μM。 优化研究表明,microLTP 处理时间和外部高压功率幅度会显著影响 ROS 的产生。在相同条件下,ROS 丰度顺序为:H₂O₂ > O₂⁻ > ¹O₂ > •OH。通过调控 microLTP 参数可生成特定浓度范围的 ROS,为后续实验确定了 ROS 生成的最佳条件。
唾液酸的深度自由基氧化
为了探索与传统氧化相比,唾液酸氧化途径及其所得产物的潜在差异。作者首先选择了 H₂O₂/UV 引发糖环裂解和 Baeyer-Villiger 重排,随后生成脱羧产物 DSA,DSA 进一步氧化为羧酸/酮类衍生物。该结果展现出与传统研究一致的化学氧化路径:H₂O₂ 对羰基进行亲核加成,随后 α-羟基过氧化物(αHHP)发生裂解(图 1a)。随后作者通过 microLTP 装置对 Neu5Ac 进行实验,发现在自由基激发时,侧链逐步氧化(羟基→醛基(步骤 I,图 1b)→羧酸(步骤 II,图 1b)同时,作者还发现了一种竞争性氧化途(步骤 III,图 1b)。虽然整个过程与化学氧化相似,但该反应过程涉及独特的侧链氧化,同时保持完整的聚糖环结构(图 1c)。正如预期的那样,步骤 III 的所得产物在充分的自由基氧化后发生最终的开环反应(步骤 IV,图 1b)。由于羟基氧化的无偏倚性,步骤 I 生成了各种结构异构体,因此很难确定最终产物结构。 为了探究反应机理,作者计算了反应中间体的自由能(图 1d-f),结果表明与不同量的 O₂ 反应时,会产生不同的稳定异构体产物和反应路径。Neu5Ac 与 Neu5Gc 的羟基差异如图 1g 所示,作者进一步测量了 Neu5Ac 与 Neu5Gc 的氧化动力学曲线,发现 Neu5Gc 因多一个羟基而表现出更强的抗氧化能力。 图 1. 发现唾液酸的自由基氧化途径 如 Scheme 2 所示,作者通过 microLTP 生成了 Neu5Ac 氧化的 46 种中间体和产物,包括侧链氧化(步骤 I–III)和环断裂(步骤 IV)的逐步路径,并通过 DFT 计算和质谱验证了各步骤的异构体及热力学稳定性。 Scheme 2. Neu5Ac 的 46 种自由基氧化产物图谱 hTF 的唾液酸化依赖性结构稳定性 作者为了探索蛋白质结构稳定性在自由基氧化影响下对唾液酸化和糖基化的依赖性,通过天然质谱和 AIU-IM-MS 进行了一系列气相展开实验(图 2a-j),对 hTF 样品进行了唾液酸化和 N-糖基化特异性酶处理(图 2k)。非变性 MS 证实,唾液酸酶能有效去除 hTF 中的唾液酸化,但 PNGase F 去除 hTF 中 N-糖的效率较低(图 2a-c)。通过鉴定酶处理产物,能够比较氧化应激下唾液酸化的效应(图 2c、f)。自由基氧化使蛋白质质量略有下降(图 2a、d)。而去除唾液酸后,氧化时蛋白质质量的常规增加进一步支持了这一推测(图 2b、e)。 传统 CIU 为 hTF 产生了不同的电荷态依赖性去折叠模式,当将数据集转换为 AIU 模式(图 2g)时,可以直接明确地比较具有不同处理的 6 个 hTF 样本的去折叠行为。通过比较氧化后 hTF 的 CCS、AIU5 和 RMSD 数据,发现唾液酸化显著提升了蛋白抗氧化的能力。 图 2. 唾液酸化和 N-糖基化对氧化应激的 hTF 结构稳定性的影响 唾液酸化 hTF 的自由基氧化曲线 为了确定唾液酸化在抗蛋白质氧化应激中的作用,作者用唾液酸酶和 PNGase F 酶处理各种 hTF 样品,以选择性去除唾液酸和 N-糖基化,然后进行 LC-MS/MS 测量以鉴定和定量自由基氧化位点。 根据酶处理后的氧化水平变化,将鉴定出的肽分为两类:上调(I)和下调(II)。I 组肽(如 47-60、531-541等)氧化水平显著上调,对自由基氧化反应性更高;II 组肽(如 70-107、123-132等)氧化程度显著降低(图 3a)。从 hTF 的 3D 结构来看(图 3b、c),I 组肽大多位于 C 端且靠近糖基化位点(Asn432 和 Asn630),说明糖基化可能对抵抗主链氧化有保护作用;而 II 组肽氧化水平降低可能是因为去除游离寡糖后结构重排造成的。这些结果进一步揭示了糖基化修饰和氧化作用在影响蛋白质结构稳定性方面的复杂相互作用。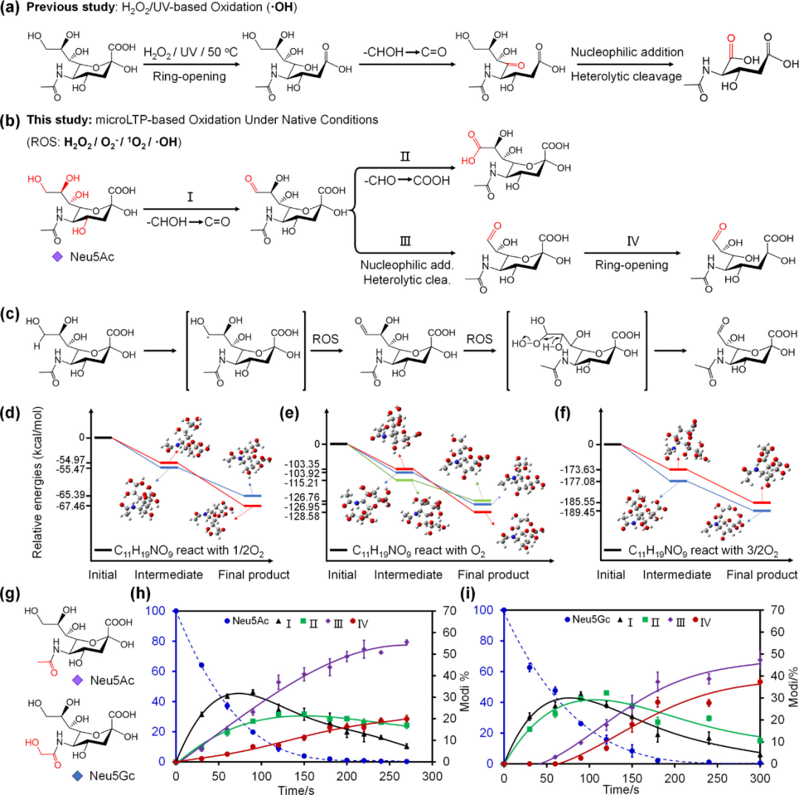
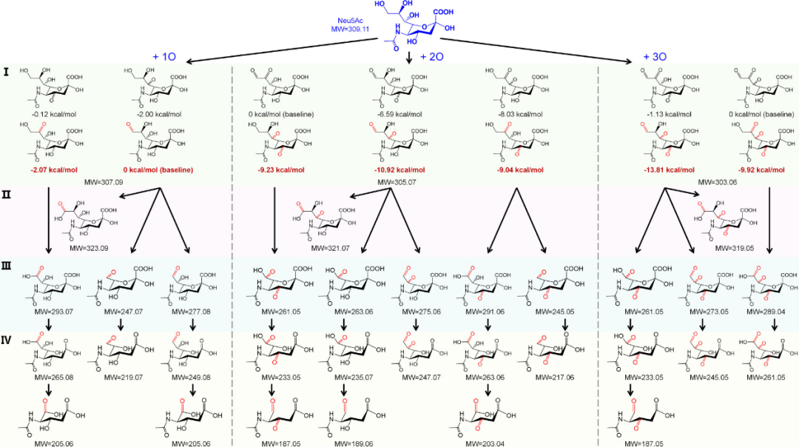
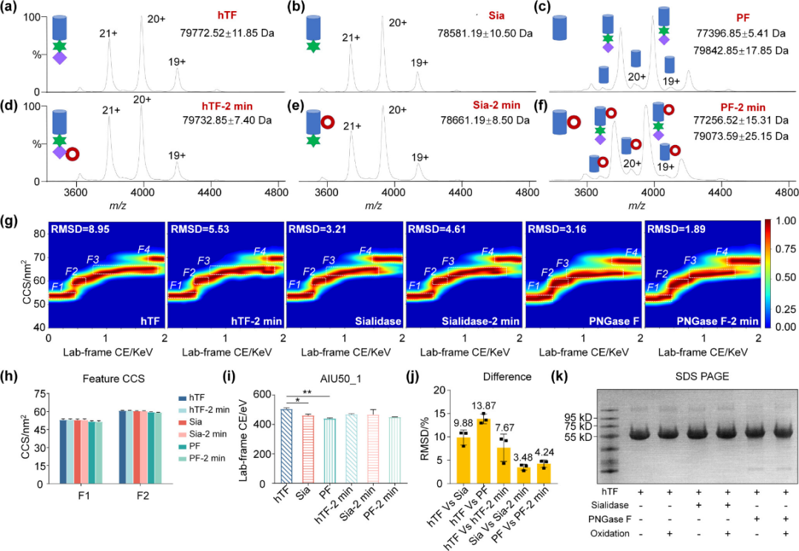
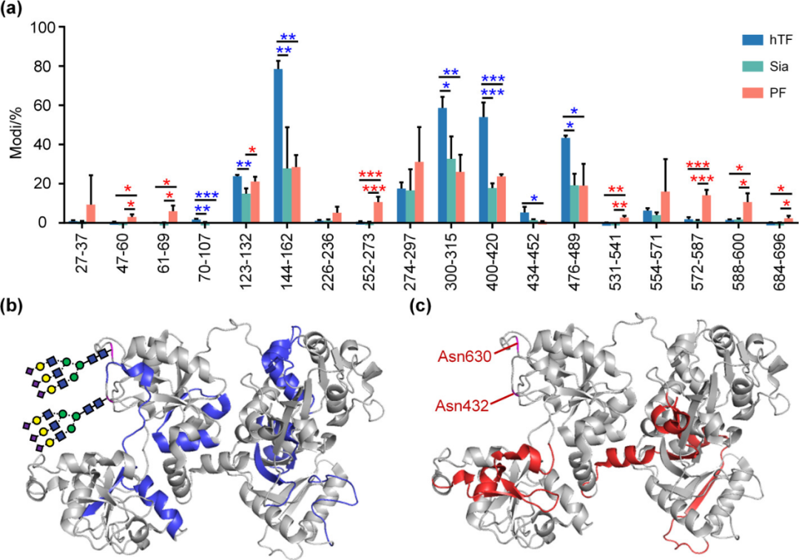
图 3. 受唾液酸化和 N-糖基化调节的 hTF 的自由基氧化曲线
此外,作者以时间分辨自由基处理方式分析了具有唾液酸化和 N-糖基化的天然 hTF 样品在不同时间(30、60 和 120 秒)的氧化位点,结果显示,蛋白质多个区域(如肽段 144-162、226-239 等)存在显著的剂量依赖性修饰(图 4a)。将氧化位点映射到 hTF 的 3D 结构中发现,N 端和其他非糖基化区域优先被氧化(图 4b)。 随后,作者还全面表征了在不同血浆处理时间下在 Asn432 和 Asn630 位点的糖型变化(图 4c、d),发现有唾液酸化的糖在 Asn432 和 Asn630 位点随时间增加而减少,且不同数量的唾液酸化糖型比例进一步证明了唾液酸化糖的氧化降解。 图 4. 天然 hTF 自由基氧化位点的时间分辨标测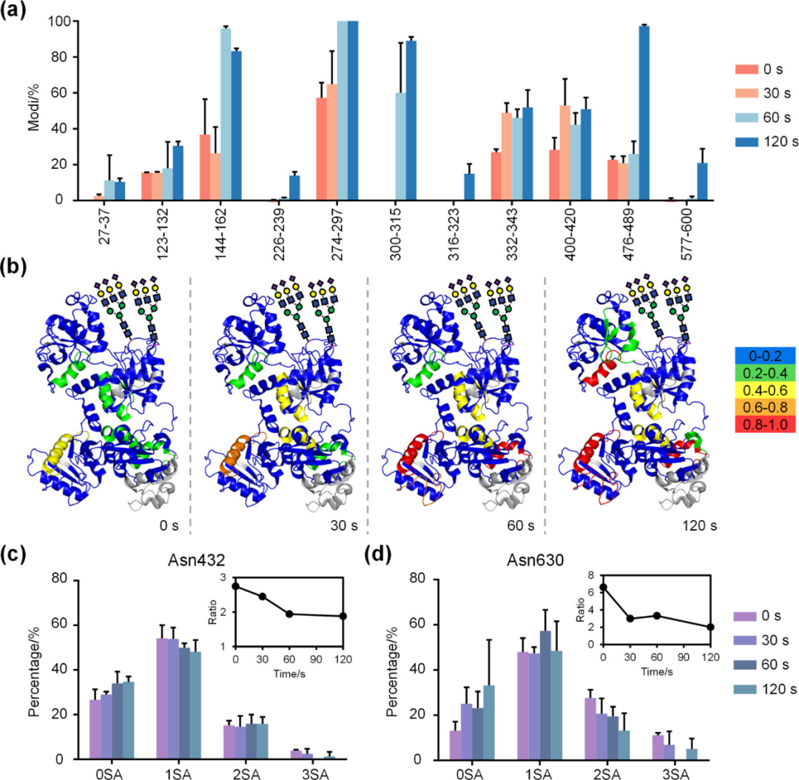
综上所述,本研究首次揭示了唾液酸化修饰在保护蛋白质结构和功能免受氧化应激损伤中的分子机制。这一发现不仅为理解糖基化在细胞应激中的作用提供了新的视角,还为开发更稳定的蛋白质药物开辟了潜在的创新方向。
———————— 本文作者:WXL 原文链接: https://pubs.acs.org/doi/10.1021/jacs.4c14454


目前评论: