- A+
卤代酮的还原脱卤是在金属还原剂存在下导致由α-卤代酮形成酮和酮的官能化衍生物的有机反应。
介绍
通过用亲电子卤素源处理,可以容易地从烯醇化物制备α-卤代酮。[2] α-卤代酮的还原产生反应性中间体,其可以表现出独特的取代模式和反应性。例如,α,α'-二卤代酮的还原产生2-氧杂烯丙基金属络合物,其作为2π组分参与[4 + 3]和[3 + 2]环加成反应。[3] 2-氧杂烯丙基金属中间体也可以在涉及α碳的过程中拦截亲核试剂。[4]此外,因为还原单卤代酮以特定位点的方式产生烯醇化物,与烯醇化物相关的反应(烷基化,醛醇,迈克尔))可以在还原条件下使用卤代酮底物进行。
(1)
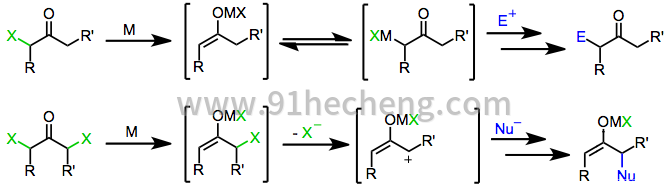
机制与立体化学
Monohalo Ketones
通过单电子和双电子还原剂还原单卤代酮,得到母体酮,用亲电试剂官能化的衍生物或二聚化产物。还原机制本身取决于还原剂的性质。
单电子还原剂,例如d 6或d 1过渡金属络合物,最初向卤代酮提供单个电子。所得自由基阴离子的碎裂产生有机基团和卤素阴离子。从第二当量还原剂中供给第二电子导致形成金属烯醇化物,其中还原剂的氧化态增加1。[5]
(2)
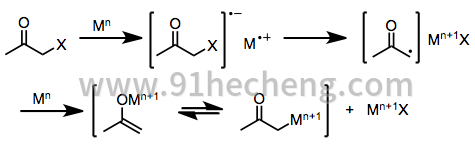
双电子还原剂,其中最突出的是锌金属,经历直接氧化加成到单卤代酮中,得到金属烯醇化物,其中金属的氧化态增加了2。随后与未反应的卤代酮的歧化有时会导致形成两当量的烯醇基,其随后可能二聚化。[6]
(3)
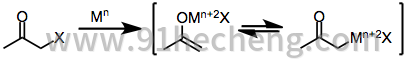
用亲电子试剂处理衍生自单电子还原剂或双电子还原剂的烯醇化物,得到α-官能化的酮作为最终产物。
α,α-二卤代酮
与单卤代酮类似,偕二卤代酮在暴露于单电子或双电子还原剂时最初形成金属烯醇化物。在质子溶剂存在下,还原在此阶段停止以提供单卤代酮(其可进一步还原为母体酮)。[7]但是,在从烯醇盐中间体,得到α酮卡宾或卡宾,其经历CH插入反应没有俘获电子试剂或质子溶剂,剩余的卤化物的损失。[8]
(4)
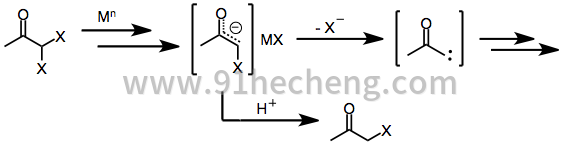
α,α'-二卤代酮
α,α'-二卤代酮的初始还原导致金属烯醇化物中间体。剩余卤化物的损失产生2-氧杂烯丙基金属络合物,其在二烯或烯烃存在下经历[4 + 3]和[3 + 2]环加成反应。[3] 2-氧杂烯丙基金属配合物异构化为环丙酮和丙二烯氧化物形式是快速和可逆的; 增加氧 - 金属键的共价特征有利于2-氧杂烯丙基异构体。[9]
(5)
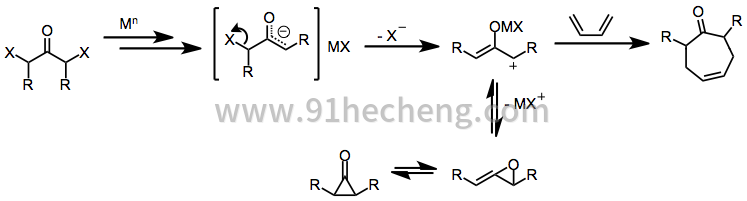
范围和限制
α-卤代酮的还原可以提供母体酮,部分还原的卤代酮,或者通过亲核试剂或亲电子试剂沿着还原途径截取中间体而产生的产物。获得的产物取决于还原剂和卤代酮的取代模式。本节描述了单卤代,α,α-二卤代和α,α'-二卤代酮的还原或还原官能化的条件。
Monohalo Ketones
单卤代酮可以用锂金属还原成相应的母体酮。[10]其它有用的减少用于该转化剂包括锂dialkylcuprates [11]和六羰基钼-氧化铝。[12]
(6)
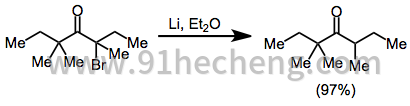
通过还原单卤代酮产生的烯醇化物的烷基化限于最具反应性的烷基卤化物。[13]然而,减少醛的存在会导致还原醛醇产物。锌粉可以单独使用或与二乙基氯化铝和催化量的溴化铜(I)一起使用。[14]
(7)
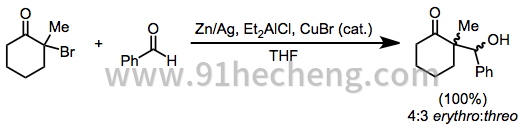
还原二聚化可以由两种中间体α-酰基的组合或金属烯醇化物对未反应的卤代酮的亲核攻击产生。尽管通常会产生复杂的反应混合物[5],但在某些情况下可能会产生选择性二聚化。在下面的例子中,产品分布依赖于溶剂[15]
(8)
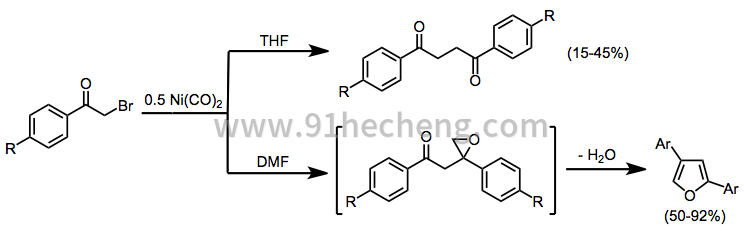
α,α-二卤代酮
取决于所用的条件,偕二卤代酮可以与有机铜酸盐还原为母体酮,单卤代酮或官能化单卤代酮。[16]温℃至室温温度导致相应的α,β不饱和酮在这些条件下产生的从-40官能α卤代酮。
(9)
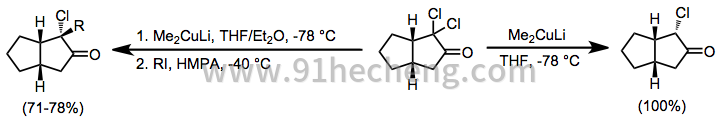
α,α'-二卤代酮
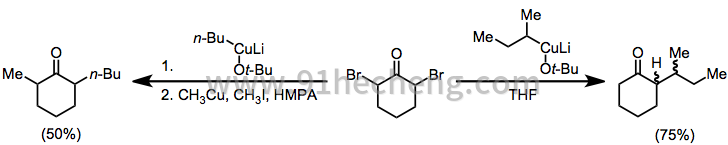
有机铜酸盐也可用于将α,α'-二卤代酮还原成烷基化酮。在不存在亲电子试剂的情况下,单烷基酮以高收率分离; [17]当加入烷基碘时,分离出二烷基酮(孪生烷基化是一个有问题的副反应)。[18]
(10)
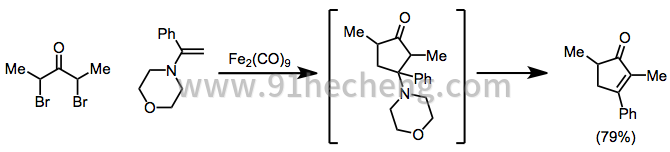
在用α(α) - 二卤代酮与铁(0)络合物还原过程中产生的2-氧杂烯丙基金属中间体参与[4 + 3]和[3 + 2]环加成反应,分别形成环庚烯酮和环戊酮。在[3 + 2]环加成反应期间,烯烃上的取代基可以消除以在一锅中从烯烃中提供环戊烯酮。[19]
(11)
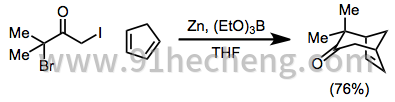
[4 + 3]环加成的范围很广[3] - 该反应可用于形成环庚烯酮,以及桥联[20]或稠合[21]多环产物。还原可以在4π组分存在下进行[22]
(12)
合成应用
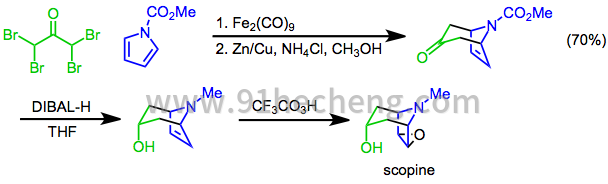
吡咯的[4 + 3]环加成可用于建立托烷生物碱的双环骨架。例如,scopine的合成使用N-甲氧基羰基吡咯和α,α,α',α'-四溴丙酮的[4 + 3]环加成作为关键步骤。用二异丁基氢化铝(DIBAL-H)进行非对映选择性还原,然后用三氟过乙酸环氧化[23],得到目标物。
(13)
实验条件和程序
典型条件
α-卤代酮可通过许多方法制备,但应在惰性气氛下冷藏,以避免分解。处理时应小心,因为α-卤代酮是lachrymators和皮肤刺激物。
大多数市售的还原剂可以原样使用或在简单纯化后使用。少数需要准备和立即使用; 这些包括锌/铜和锌/银对[24] [25]和有机铜[26]
示例程序[27]
(14)
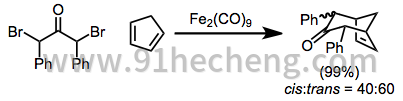
5.0g(14mmol)1,3-二溴-1,3-二苯基丙-2-酮,25g(167mmol)碘化钠,50mL(40g,606mmol)环戊二烯和150的混合物将1mL乙腈煮沸15分钟。加入氯仿,洗涤混合物,先用硫代硫酸钠溶液洗涤,然后用水洗涤,用硫酸钠干燥。浓缩得到粗物质,将其在长柱硅胶上进行色谱分离,得到7.4g(99%)2α,4α-和2α,4β-二苯基双环[3.2.1]辛-6-烯-3的混合物。通过IR光谱判断,比例为40:60。从乙醇中结晶主要产生顺式异构体作为第一批晶体,并且来自丙酮的母液中的物质结晶主要产生反式异构体。顺式加合物在149.5-151.5°(从乙醇)熔化:IR(Nujol)cm -1:1700,755,740,705 。反式加合物在134-136°熔化(来自丙酮); IR(Nujol)cm -1:1700,1665,750,740,700。


目前评论: