- A+
烯烃的合成是有机化学中一个长期关注的话题,许多烯烃的合成方法已经发展起来,其中Wittig反应和烯烃的复分解是应用最广泛的。然而,高选择性合成多取代烯烃仍然是一个巨大的挑战。近年来,过渡金属催化炔烃碳金属化作为一种合成多取代烯烃的有效方法而受到越来越多的关注。与其他金属试剂相比,锌试剂具有显著的优势,对炔烃碳锌化反应的研究具有重要意义。
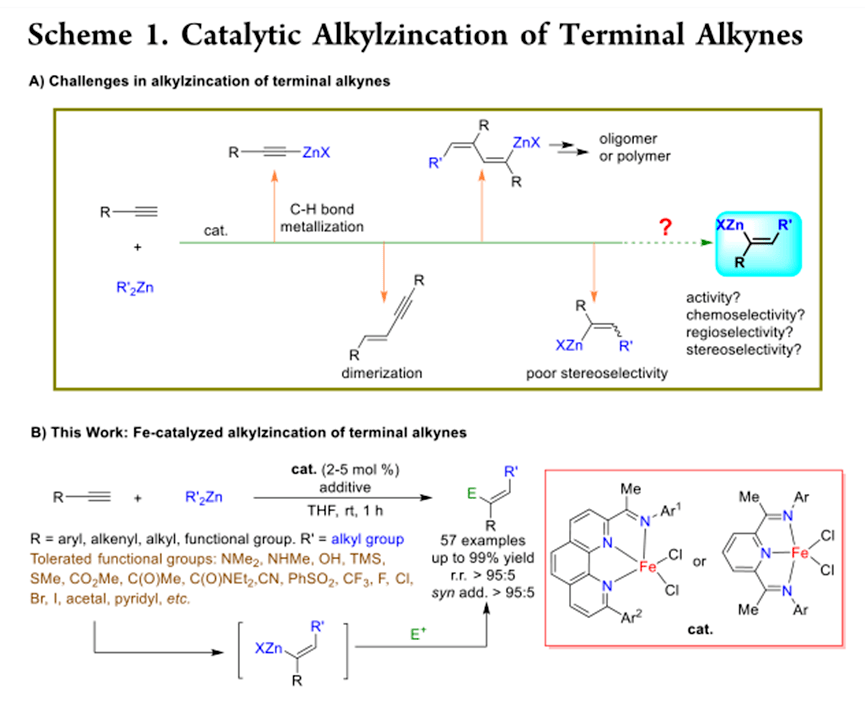
末端炔碳锌化的主要挑战如下(方案1A): (1) 炔烃的强酸性质子可以淬灭反应或降低其化学选择性; (2) 炔烃的C-H键容易与过渡金属催化剂发生氧化加成反应,随后二聚形成烯炔副产物; (3) 炔烃容易发生多次碳化反应,生成二烯基或多烯基金属物质,导致炔烃低聚产物的形成; (4) 锌试剂容易产生自由基,难以控制反应的立体选择性。由于上述挑战,过渡金属催化末端炔烃的碳化反应领域的进展非常有限。
2012年,Corpet和Gosmini使用钴-联吡啶配合物催化苯乙炔和溴化苯锌之间的顺式苯锌化反应。仅报道了一个例子,并且烯基锌产物的产率尚未确定。 2015 年,Hu和同事报道了使用化学计量锌作为还原剂的烷基卤化物和芳基乙炔之间的铁催化还原偶联反应。机理研究表明,该反应涉及自由基反式加成,生成的 (E)-烯基锌物质被末端炔烃的 C-H 键部分淬灭。作者在此报告了一种通过带有三齿 1,10-菲咯啉-亚胺或吡啶二亚胺配体的铁配合物催化末端炔烃的烷基锌化方法的开发(方案1B)。本工作中使用的铁催化剂表现出Z立体选择性,这与Hu和同事报道的催化剂不同。作者首次实现了烯基乙炔、烷基乙炔和功能化乙炔的烷基锌化。
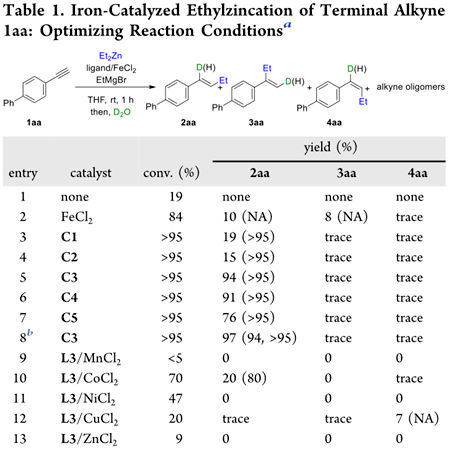
作者首先使用 4-苯基苯乙炔 (1aa) 作为模型底物,在室温下于THF中与 Et2Zn 反应(表1)。对照实验表明,在没有催化剂的情况下,所需的反应无法进行(条目1)。当FeCl2为催化剂时,反应显示出较差的化学和区域选择性,并产生低产率的乙基锌化产物2aa和3aa以及炔烃低聚副产物(条目2)。作者评估了几种可用于炔烃羰基化的催化剂,包括铁、钴和镍盐或其配合物,但没有一个反应以 >12% 的产率提供所需的乙基锌化产物 2aa。
接下来,作者在 EtMgBr 作为添加剂的情况下系统地评估了FeCl2与各种配体的配合物。具有二齿氮配体、单膦配体、双膦配体和三齿配体的催化剂PNN 配体的转化率很差,仅提供痕量的乙基锌化产物。使用具有三齿菲咯啉-亚胺配体 (C1-C3) 的铁催化剂导致炔烃的完全转化(条目 3-5),但未取代的催化剂 C1 和 3,5-二叔丁基苯基取代的催化剂 C2 得到低2aa 的产率以及炔烃低聚或聚合副产物(表 1,条目 3 和 4)。相比之下,C3 在 C9 上具有庞大的 2,4,6 -三异丙基苯基,其 2aa 的产率接近定量,具有高区域和立体选择性(表 1,条目 5)。此外,具有吡啶二亚胺配体的 C4 和 C5 也显示出良好的活性和选择性(表 1,条目 6 和 7)。
接下来,作者使用 C3 作为催化剂来筛选反应条件。发现没有添加剂只能获得中等产量。使用LiCl作为添加剂得到了令人满意的结果。在最佳反应条件下,目标产物 2aa 得到97% 的NMR产率和 94% 的分离产率(条目 8)。该反应可以放大至克级,收率保持在 91%。作者还评估了其他金属配合物作为催化剂,但所有测试的配合物都表现不佳(表 1,条目 9-13)。
使用最佳条件(表 1,条目 8),作者研究了反应的底物范围(方案 2 和 3)。

接下来,作者筛选了其他常用的锌试剂,以及末端炔烃与 Me2Zn、nPr2Zn、nBu2Zn 的反应。二戊基锌和双(戊-4-烯-1-基)锌以中等至良好的收率平稳地提供了相应的产物2ca-2cg,具有高立体选择性。
作者成功地将反应扩展到共轭炔烃底物(方案3A)。反应条件的系统优化表明,以 C5 作为催化剂,PhCF3 作为溶剂的反应表现出最好的结果。芳基和烷基取代的烯炔分别以高产率和高区域选择性和立体选择性提供共轭二烯 2da 和 2db。烷基乙炔也顺利地进行了 C5 催化的乙基锌化反应,以高产率和高区域选择性提供所需的产物(方案 3B)。出乎意料的是,O-、N-、S-和Si-取代的乙炔顺利地进行了烷基锌化反应,以中等至良好的收率得到相应的产物(2fa-2fd)(方案3C)。
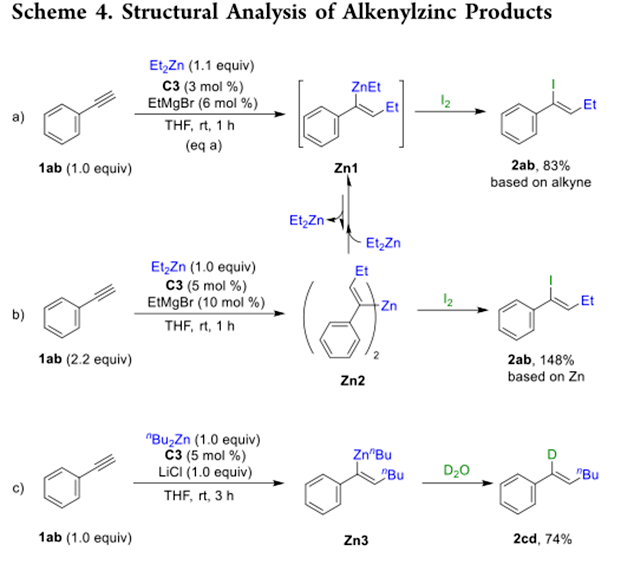
作者还阐明了烯基锌产品的结构。
为了证明当前方案的潜在合成应用,作者对烯基锌产物 2aa' 进行了各种转化(方案 5A)。 该化合物是合成三取代烯烃的有用中间体。由于(烷基)(烯基)锌试剂很容易发生氧化偶联,羧基化产物通常在发生偶联反应之前转化为烯基碘化合物。相比之下,作者方法制备的二烯基锌试剂 Zn2 可以直接与 4-碘硝基苯发生 Negishi 偶联以 85% 的产率提供 T1 并保留配置(方案 5A-a)。铜盐促进的 2aa' 的碳-锌键烯丙基化、酰化和炔基化反应以良好的收率立体选择地提供官能化三取代烯烃 T2-T4(方案 5A-b-d)。2aa'与苯甲醛和丙炔酸甲酯的加成反应分别立体特异性地产生多取代的烯丙醇T5和共轭二烯T6(方案5A-e,f)。 2aa' 与异氰酸酯和二氧化硫的加成反应分别以 92% 和 39% 的收率提供了 C-Zn 键酰胺化和磺化产物 T7 和 T8(方案 5A-g,h)。
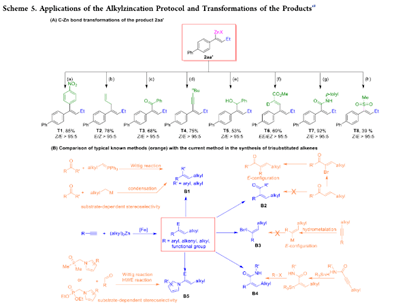
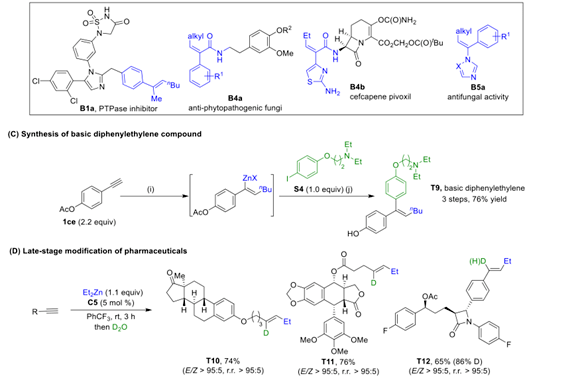
在实现了烯基锌产物 2aa' 的上述转化后,作者将方案与制备三取代烯烃的典型已知方法进行了比较(方案 5B)。作者还使用铁催化烷基锌化方法合成了化合物 T9,该化合物具有细胞毒性和抗雌激素活性 28(方案 5C)。作者还成功地使用铁催化烷基锌化方法对几种药物分子进行后期修饰,包括雌酮、鬼臼毒素和依折麦布衍生物(方案 5D)。
总之,作者开发了一种使用三齿菲咯啉-亚胺和吡啶二亚胺配体修饰的铁催化剂对末端炔烃进行烷基锌化的方法。该方法以高产率直接获得烯基锌化合物,具有高化学、区域和立体选择性,并显示出良好的官能团耐受性和广泛的底物范围。烯基、烷基和杂原子取代的乙炔。结合产物的 C-Zn 键的转变,该方法为获得各种三取代烯烃和生物活性分子提供了有效、实用的途径。
DOI:10.1021/acscatal.1c05870


目前评论: