- A+
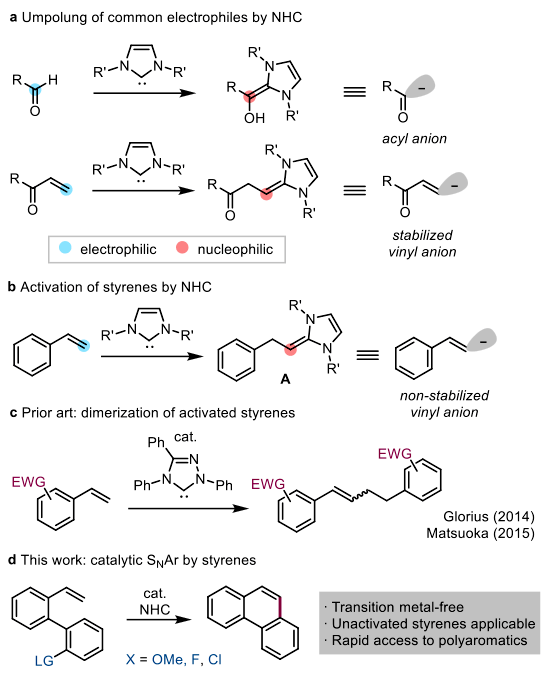
NHC最常见的活化方式是由醛生成Breslow中间体,使亲电的羰基碳充当亲核试剂。α,β-不饱和羰基化合物也可以被活化,生成了脱氧- Breslow中间体(Figure 1a)。以上例子表明NHC可以激活非羰基不饱和键,催化形成乙烯基阴离子(Figure 1b)。Glorius和Matsuoka独立报道了缺电子苯乙烯可以通过由三唑基NHC催化形成一种叶立德中间体的二聚反应(Figure 1c)。然而,这种二聚反应是苯乙烯衍生物被NHC活化唯一报道的例子,中间体A的合成潜力几乎未被探索。在此,作者报道了NHC对未活化苯乙烯的亲核活化及其在催化SNAr反应中的应用。
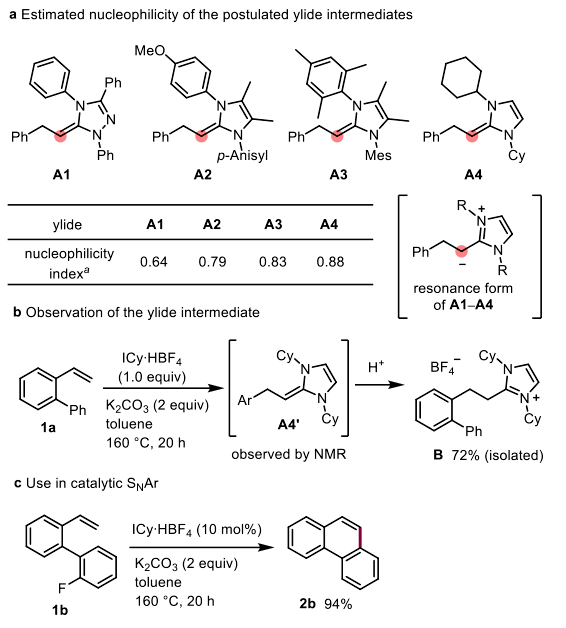
作者发现在160℃,三唑NHC催化下,仅得到45%的苯乙烯-NHC加成产物,没有得到二聚产物,这表明提高NHC本身的亲和性以及苯乙烯-NHC叶立德中间体的亲和性对反应很重要。因此,作者研究了一系列苯乙烯-NHC叶立德中间体的亲核指数(Figure 2a)。结果表明A4具有最强的亲和性,并且可以以74%收率得到苯乙烯-NHC中间体。通过该中间体,作者开发了催化分子内SNAr反应(Figure 2c)。
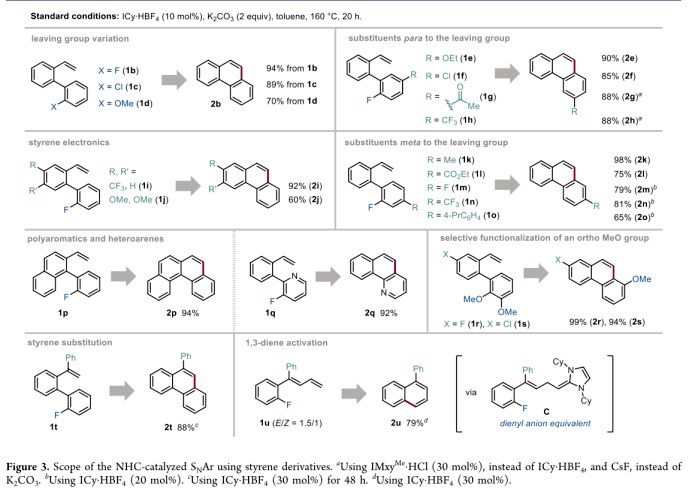
在确定最佳反应条件后,作者对反应底物范围进行了研究。发现对氟离去基团效果最好。对不同的苯乙烯衍生物均可以进行反应获得菲衍生物,获得不错的收率。
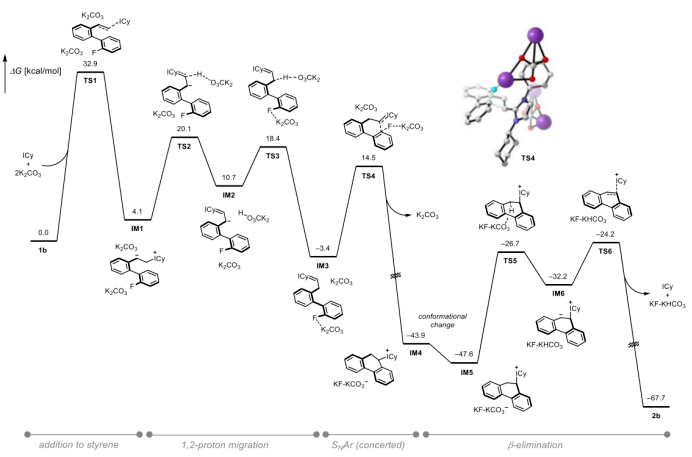
接下来作者进行了DFT计算,对反应机理进行了研究。TS1能垒较高,因此反应需要高温来激活,IM1通过分步质子迁移获得叶立德中间体,而不是一步得到。随后的亲核芳香族取代是通过TS4协同反应得到,IM4中ICy的β消除是通过IM6的E1cB机制发生的。详细反映机理见上图。
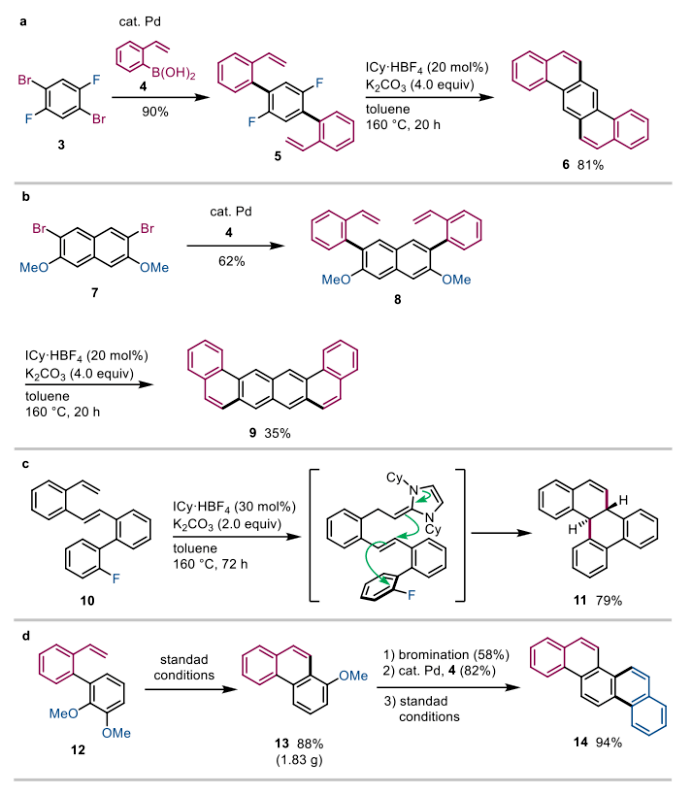
最后作者通过该反应合成了一系列稠环芳烃,以上例子证明了苯乙烯活化方法在选择性构建多芳香族骨架中的强大潜力。
总之,作者报道了一种利用NHC进行苯乙烯亲核活化的方法,以及在分子内SNAr反应中的成功应用。瞬态叶立德中间体具有充分的亲核性,能够攻击芳氟化合物、氯化物和甲氧化物。结果表明,该方法适用于一系列多芳香族化合物的合成。
DOI:10.1021/jacs.2c02579


目前评论: